Tulemused
Kirjeldav analüüs
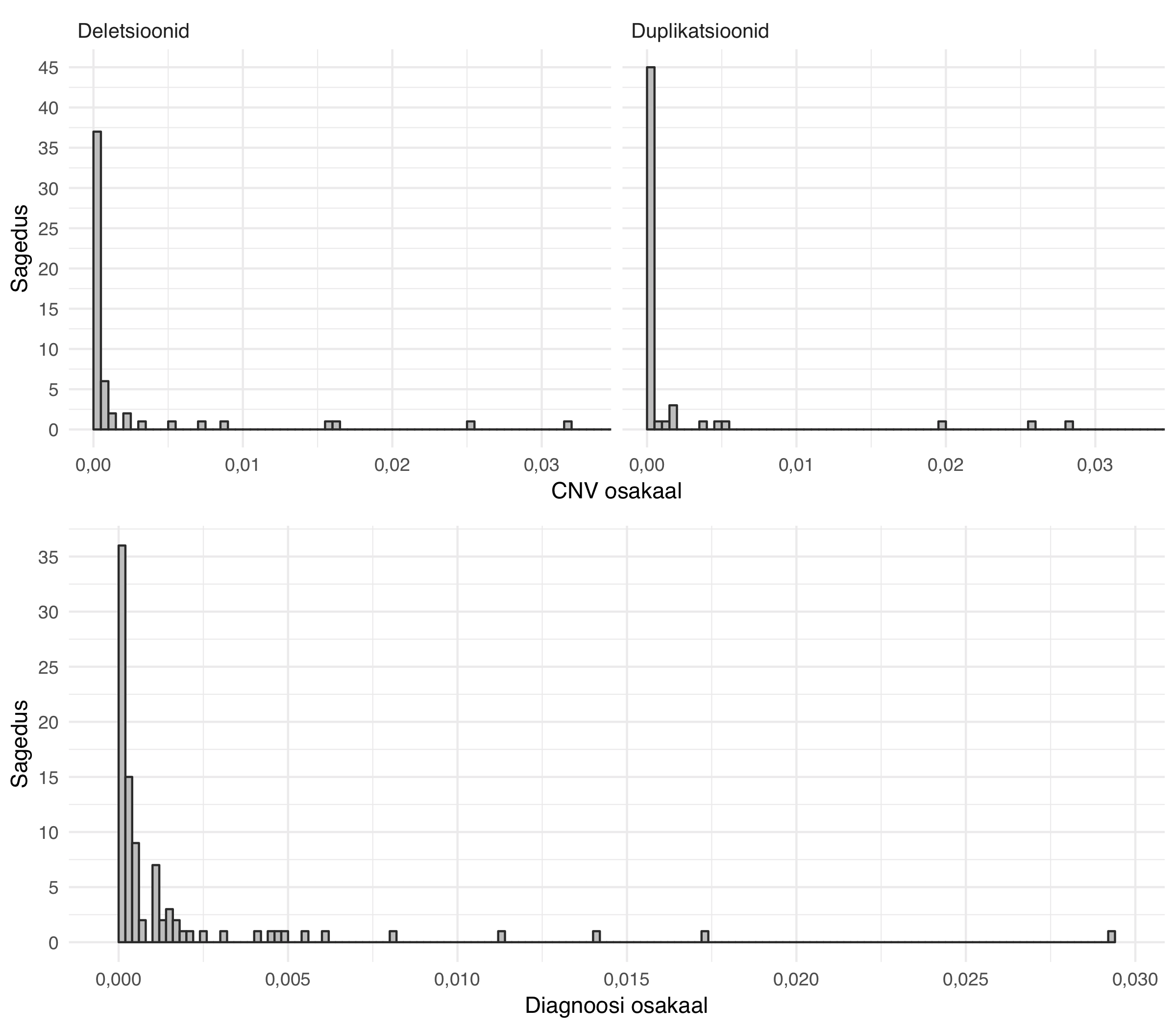
TÜ EGV andmestikus, millest sugulased on välja jäetud, on kokku \(32999\) geenidoonori andmed. TÜ EGV doonoritel on CNV-sid ülekattes \(56\) erineva farmakogeeniga. Enamike farmakogeenidega on ülekattes väga vähe CNV-sid.
Keskmine deletsioonide suhteline sagedus geenide kaupa on \(0.525\%\) ja duplikatsioonide suhteline sagedus geenide kaupa on \(0.174\%\). Seejuures on \(32\) farmakogeeni puhul deletsioonide osakaal alla \(0.1\%\) ning \(36\) farmakogeeni puhul on duplikatsioonide osakaal alla \(0.1\%\).
Harvad on ka ravimi kõrvaltoimete diagnoosid. Keskmine diagnooside suhteline sagedus on \(0.167\%\) ning \(63\) diagnoosi esinevad vähem kui \(0.1\%\) doonoritest
Simulatsioonid
CNV kvaliteediskoor parandab statistilist võimsust
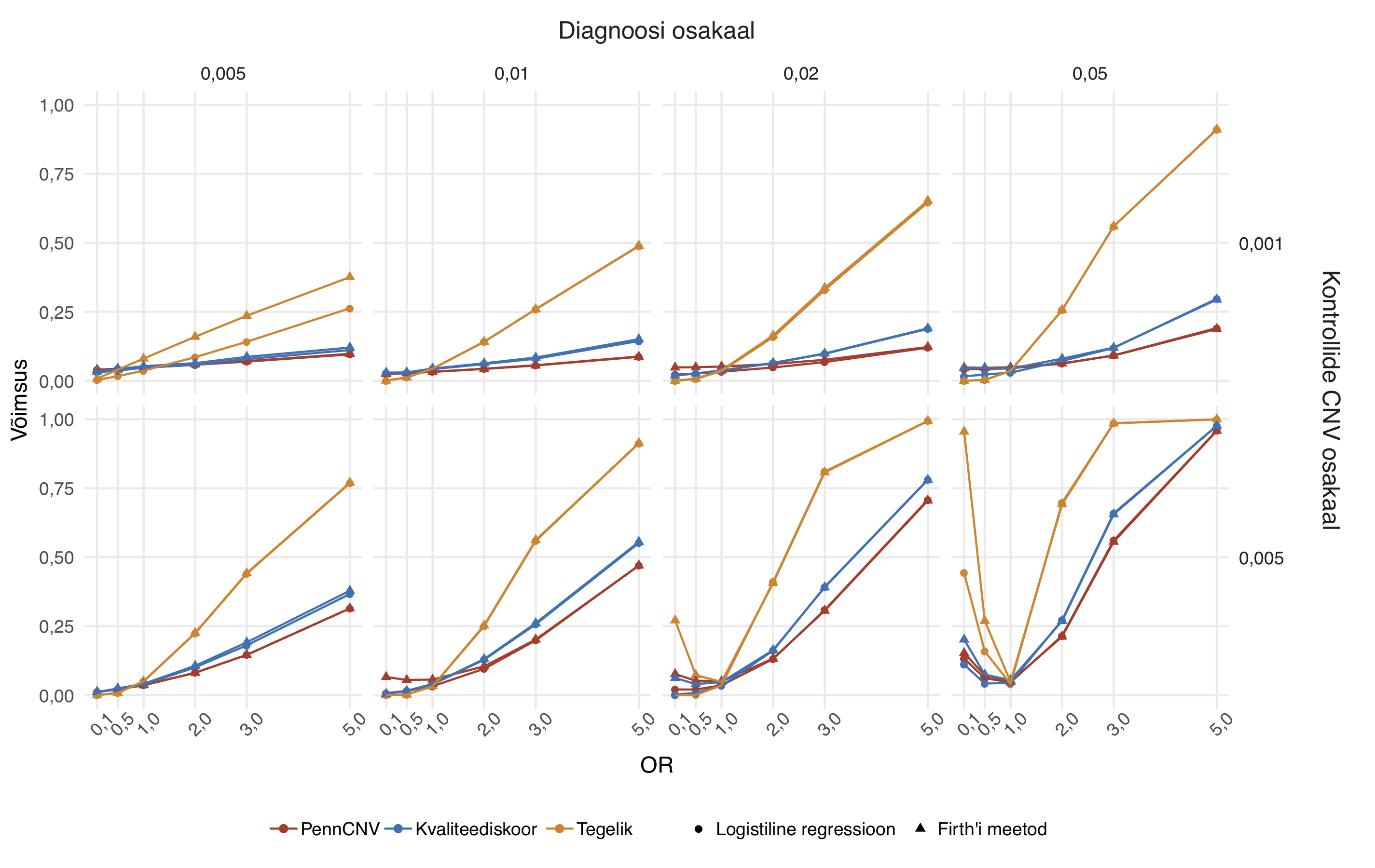
Simulatsioonid viidi läbi erinevate kontrollide CNV osakaalude \(p_0 \in (0.001; 0.005; 0.01; 0.02)\) ja ravimi kõrvaltoimete osakaalude \(p \in (0.001; 0.005; 0.01; 0.02; 0.05)\) korral. Need osakaalud määrati vastavalt TÜ EGV ja UKB diagnooside ning CNV-de osakaalude jaotuste järgi (vt ülaltoodud joonis). Simulatsioonide jaoks eeldati, et šansside suhted \(OR \in (0.1; 0.5; 1; 2; 3; 5)\) ning valimimahuks valiti \(33000\) (valimimaht TÜ EGV andmetes pärast sugulaste eemaldamist).
Simulatsioonide tulemused näitasid oodatavalt, et tegeliku CNV mitteteadmine vähendab oluliselt testimise võimsust. Samuti on näha, et kvaliteediskoori kasutamine PennCNV tunnuse asemel parandab testimise võimsust madala CNV sageduse korral.
Sageduspiiride määramine
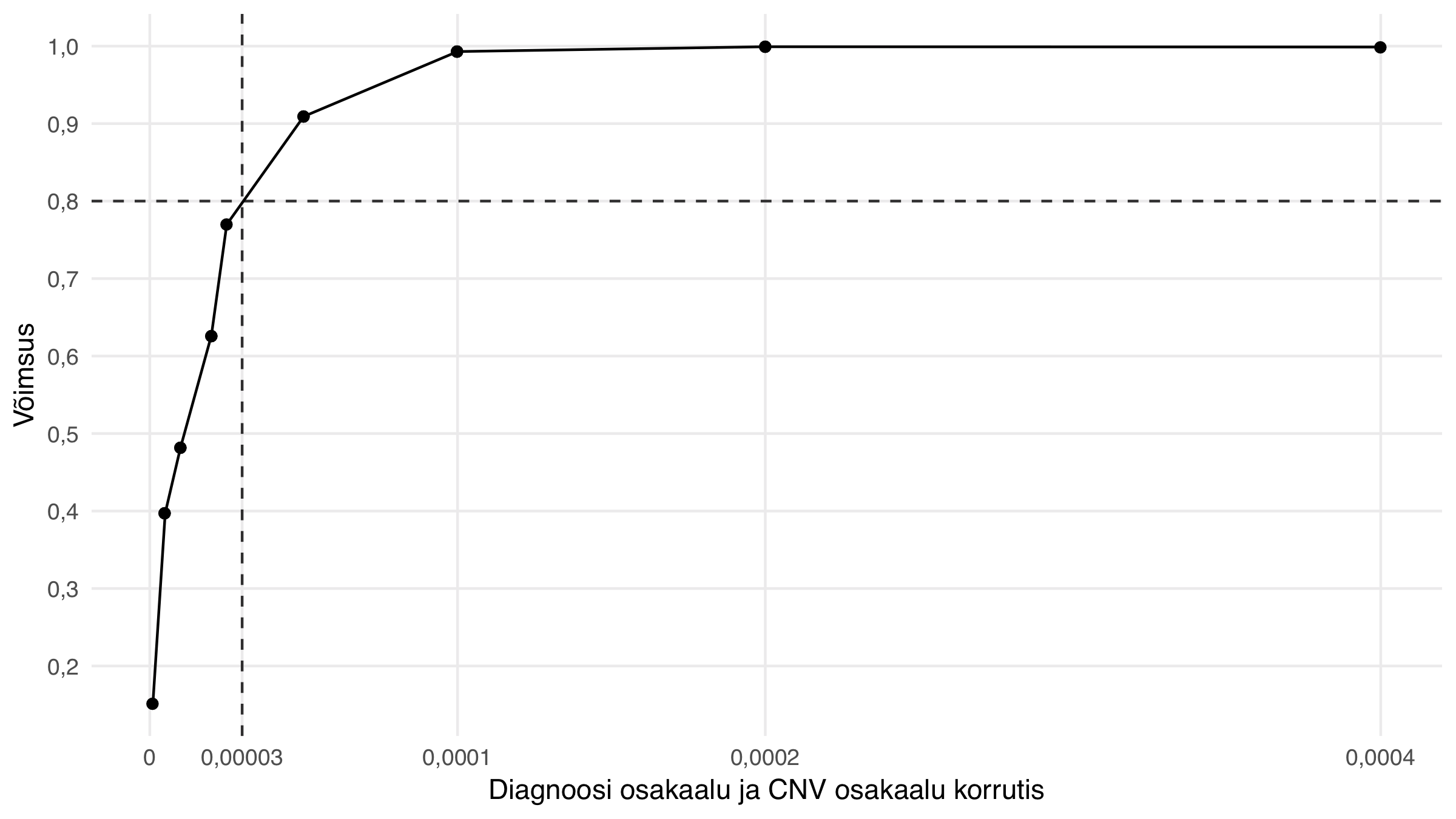
Tuvastamaks potentsiaalselt suuri efekte, määratakse CNV piirsagedused nii, et testimise võimsus olulisuse nivool \(0.05\) oleks vähemalt \(80\%\) olukorras, kus tegelik CNV on teada ja tegelik šansside suhe on \(5\). CNV ja diagnoosi osakaalu korraga arvessevõtmiseks kasutatakse piiride määramiseks nende osakaalude korrutist. Alljärgnevalt jooniselt näeme, et \(80\%\) võimsuse saavutamiseks peab vastav korrutis olema vähemalt \(3 \cdot 10^{-5}\). Sellise piiri kasutamisel jääb alles vaid \(270\) testi \(10000\) võimalikust.
Kõrvaltoimete analüüs
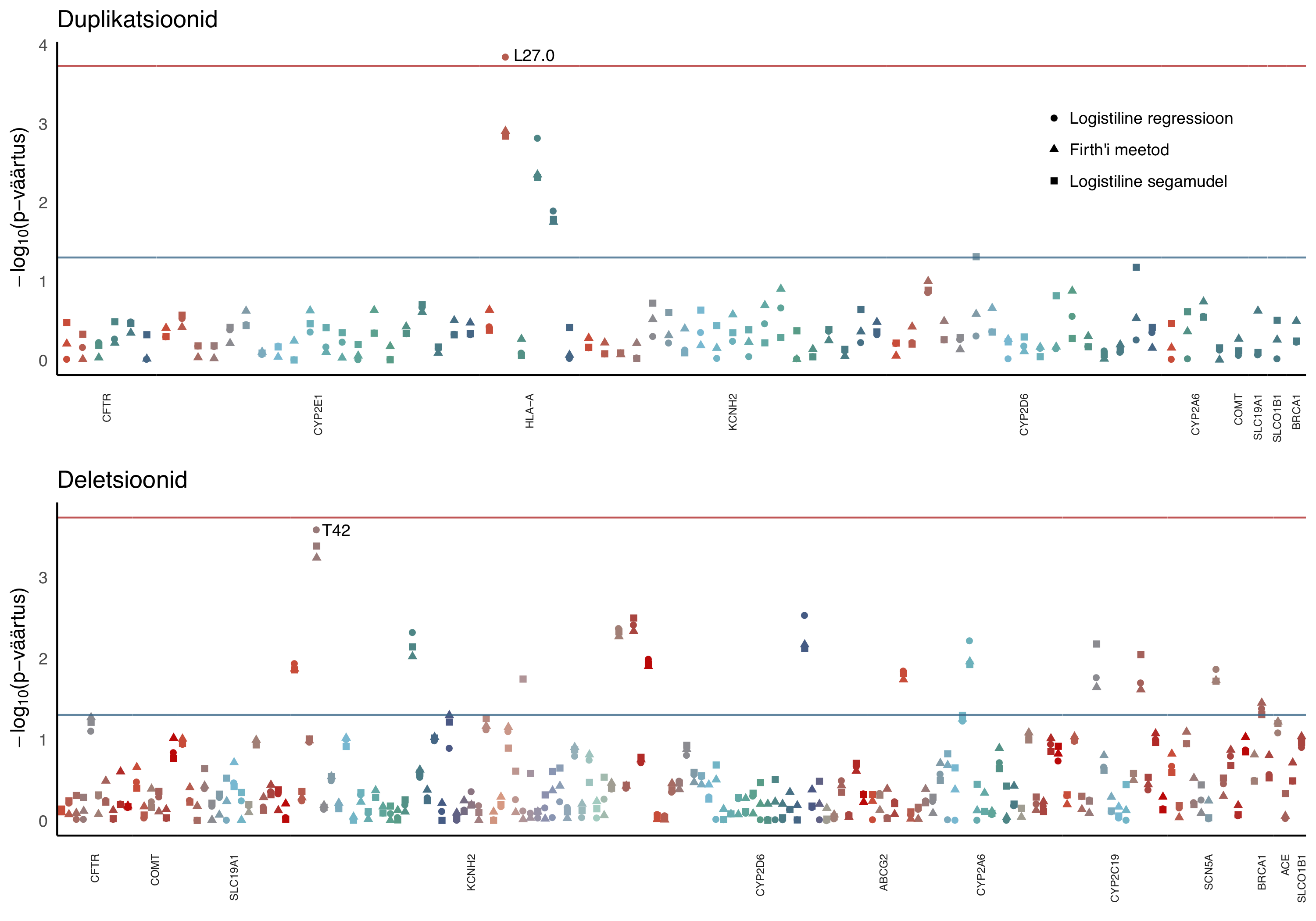
Alljärgnevalt on toodud testide p-väärtused TÜ EGV andmete korral. Punktid on värvitud diagnooside järgi ning iga punktikolmik tähistab ühte testitud CNV-diagnoos paari. Punane joon vastab korrigeeritud olulisuse nivoole \(0.000185\) ning sinine joon olulisuse nivoole \(0.05\).
Duplikatsioonide korral on korrigeeritud olulisuse nivoo suhtes oluline seos HLA-A ja L27.0 (rohtudest ja ravimitest tingitud üldine nahalööve) vahel.
Deletsioonide korral on korrigeeritud olulisuse nivoole kõige lähemal KCNH2 ja T42 (Mürgistus antiepileptikumide, sedatiiv-hüpnootiliste ja parkinsonismivastaste ravimitega) testi p-väärtus.
Arutelu
Varem on väga mitmeid erinevaid HLA-piirkondi (kuhu kuulub ka HLA-A geen) seostatud ravimist tingitud ülitundlikkusreaktsioonide tekkimisega. Täpne mehhanism, kuidas HLA-A mõjutab ravimist ülitundlikkuse tekkimist, ei ole kindlalt teada, kuid ilmselt võivad muutused HLA-A geenis põhjustada ravimiaine esitlemist T-rakkudele, mis osalevad organismile immunoloogilise kaitse andmises. Nende muutuste tulemusena tekib ülitundlikkusreaktsioon.